Patologie e danno ossidativo: causa o effetto?
(prof. F. Marotta)
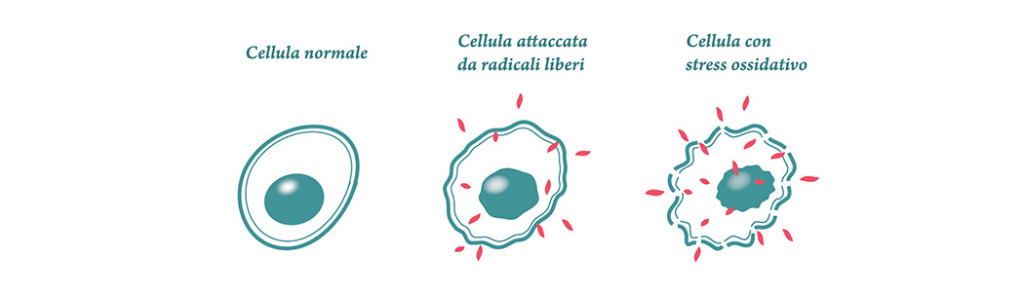
Se lo Stress Ossidativo sia epifenomeno o primum movens di patologia non è cosa facile a dirsi: certo è che, essendo possibile causa di ulteriore danno, questo fenomeno patogenetico va in ogni caso contrastato (Figura 1).
Nel corso dell’evoluzione, se la genomica non è profondamente cambiata, l’alimentazione umana ha invece subito radicali mutamenti (Figura 2) non privi di effetti epigenetici.
Basti pensare all’allungamento delle aspettative di vita: il solo “invecchiamento” del DNA è causa di alterazioni cromosomiche progressive (Figura 3). Proprio per tale ragione importanti agenzie governative statunitensi da tempo lavorano a programmi nutrizionali e ricorrono ad implementazioni nutraceutiche allo scopo di prevenire o rallentare le patologie età-correlate (Figura 4).
Oltre all’alimentazione, nel corso dell’evoluzione anche l’ambiente ha subito profondi cambiamenti con un forte incremento della presenza di inquinanti di varia natura che vengono solo in parte monitorati in quanto solo per pochi di essi la pericolosità per la salute umana è stata studiata e documentata (Figura 5). Molte sono le evidenze della loro implicazione nella patogenesi di malattie croniche la cui rilevanza è sottolineata dal fatto che più del 80% della spesa sanitaria dei paesi occidentali è attualmente destinata per contrastarle (Figura 6).
INQUINAMENTO E STRESS OSSIDATIVO:
Ripetutamente è stato riportato in letteratura che l’esposizione agli inquinanti è causa di Stress Ossidativo (Figure 7-8): alcuni Autori hanno anche dimostrato che l’etnia caucasica ne subisce i maggiori effetti a motivo di una subottimale capacità di detossificazione (Figura 9). A conferma di ciò, è stato anche dimostrato che ben il 50% della popolazione caucasica è un “acetilatore lento”, non esprime il gene GSTM-1 e frequentemente dimostra scarsa efficacia nei meccanismi di DNA-reparing (Figura 10). La relazione tra inquinamento e Stress Ossidativo risulta essere quindi molto stretta.
Se a ciò si aggiunge la maggiore esposizione agli inquinanti ambientali rispetto ad altri, è possibile giustificare la presenza di una maggiore frequenza di alterazioni del DNA proprio nella popolazione caucasica.
Quando uno stesso evento patogenetico (noxa) determina un’alterazione dell’omeostasi cellulare, il tessuto passa ad un primo stato di attivazione su cui possono successivamente incidere tanto modificatori genetici quanto modificatori ambientali (es. inquinanti, nutrizione) in grado di generare ulteriori stati di attivazione genetica e di causare espressioni cliniche diverse (Figura 11).
Lo Stress Ossidativo è una noxa in grado di causare danno cellulare prima e sistemico poi. Fattori genetici, ambientali, alimentari, agenti infettivi, ormoni sono causa di produzione di specie reattive dell’ossigeno (ROS): se non opportunamente contrastati, i ROS inducono fenomeni infiammatori che auto-alimentano il processo che diviene un circolo vizioso che da alcuni Autori definito “inflamaging” (Figure 12-18).
Numerose e fortemente contrastanti sono state le esperienze pubblicate sull’impiego di antiossidanti nella terapia: denominatore comune, quasi invariantemente, il ricorso a molecole non naturali ma di sintesi.
Solo dal 2011 si è iniziato a parlare di sostanze nutraceutiche, neologismo volto a definire composti di natura alimentare che, oltre a compensare stati carenziali sono in grado di offrire comprovati vantaggi per la salute documentati da un dossier scientifico riconosciuto ed approvato (Figura 19). Purtroppo in Europa e in Italia la distinzione tra semplice integratore alimentare e nutraceutico resta a tutt’oggi vaga.
Molti anni di studi evidence-based sono stati dedicati all’impiego nutraceutico della papaia fermentata (FPP): potente attivatore dei macrofagi, in vitro è in grado di incrementare la sintesi di NO e TNF-alfa, di esercitare azione di scavenging degli ossidrili e di chelazione del ferro con conseguente prevenzione del danno ossidativo su DNA e proteine (Packer, 2000). Si è anche dimostrato che l’FPP promuove una protezione nei confronti del danno della mucosa gastrica etanolo-indotto e del DNA nella cirrosi epatica (Marotta, 1999). Importanti studi sono stati condotti anche nella immuno-stimolazione nei pazienti affetti da HIV (Montagnier, 1998) (Figura 20).
Numerose pubblicazioni relative a diversi stati fisiopatologici con Stress Ossidativo (Figura 21) hanno dimostrato che FPP non è un antiossidante ma agisce come un modulatore del bilancio redox. In uno studio del 2006, la somministrazione di FPP alla dose di 6 g/die in soggetti sani over 65 ha dimostrato un significativo decremento del livello di addotti DNA e del rapporto 8OHdG/dG nei soli soggetti GSTM-, un polimorfismo genico in grado di assicurare minore efficacia di risposta allo stress ossidativo rispetto ai GSTM1+ (Figura 22).
Sempre nello stesso anno è stato pubblicato un lavoro sulla suscettibilità età-correlata degli eritrociti allo Stress Ossidativo: mediante il dosaggio dei TBARS, è stato dimostrato che la somministrazione di FPP è in grado di ridurre la lipoperossidazione del globulo rosso “in toto” ma non della membrana e che la deformabilità cellulare migliora nei trattati rispetto ai placebo. Si spera che questo dato oggettivo possa essere in futuro utilizzato nella terapia della beta-talassemia (Figure 23-27).
Altri studi condotti sui globuli rossi hanno dimostrato che FPP può diminuire la lisi cellulare(Amer 2008, Figura 28), ridurre la presenza endocellualre di ROS ed aumentare quella di glutatione ridotto (Rachmilewitz 2010, Figura 29).
Le heat shock proteins 70 (HSP70) sono una classe di proteine i cui livelli plasmatici incrementano tipicamente nelle infezioni acute e nella malattia di Parkinson: valori molto elevati rappresentano pertanto un marcatore di danno cellulare.
Livelli bassi o molto bassi di HSP70 sono invece indicativi di un’inerzia cellulare alla risposta all’insulto ossidativo: a riprova di questo fatto, i livelli plasmatici fisiologici di HSP70 sono più elevati nel giovane rispetto all’anziano.
Al contrario, i livelli di IL-6 e TNF-alfa sono fisiologicamente più elevati nell’anziano. La somministrazione di FPP in soggetti anziani con polimorfismo 174GC- (pro-infiammatorio) è in grado di determinare un decremento dei livelli di IL-6 e TNF-alfa ed un incremento delle HSP70 con un complessivo ribilanciamento dell’equilibrio redox dimostrato anche con studi del rapporto glutatione e cisteina ossidata/ridotta (Figure 30-31).
Nelle epatopatie, il trattamento con FPP normalizza i livelli plasmatici di tioredoxina (Figura 32): negli epatociti stimolati in vitro con LPS il fenomeno infiammatorio indotto è attenuato in presenza di FPP (Figura 33).
Anche la qualità della vita delle persone ha importanti effetti sul bilancio redox. Uno studio del 2004 condotto sui care-givers di pazienti con patologie croniche e neurodegenerative ha dimostrato in essi la presenza di elevati livelli di stress ossidativo e di attività della telomerasi conseguenti alle difficoltà della vita da essi condotta (Figura 34). Basta talvolta un lieve stress psichico, come ad esempio una sessione di esami universitari, per determinare decrementi della barriera antiossidante (Figura 35). Effetti molto importanti sull’infertilità maschile (alterazioni del DNA e della membrana dello spermatozoo) sono determinati dagli stessi agenti in grado di indurre stress ossidativo come stile di vita, inquinanti, infezioni e patologie croniche (Figura 36).
Il trattamento dello stress occupazionale con FPP ha evidenziato effetti modulatori con evidenti diminuzioni dei livelli endogeni dei marcatori di stress: malondialdeide (MDA), metaboliti ossidati della bilirubina (BOMs), 8-OHdG (Figure 37-42). Uno studio ha dimostrato la up-regulation indotta da FPP sul gene della emossigenasi (HO) (Figura 43).
In uno studio del 2002 condotto su soggetti sani fumatori e non fumatori che valutava un marcatore di lisi eritrocitaria, l’HT50 e, conseguentemente, di integrità della funzionalità di membrana, il fattore stress psicologico è risultato sorprendentemente più dannoso dello stesso fumo di sigaretta per tutte le classi di età (Figura 44).
Più recentemente gli studi sull’effetto patogenetico dello stress ambientale ed occupazionale hanno cercato di valutare l’effetto sinergico di tre fondamentali fattori, le cosiddette “omiche”: esposomica (fattori esterni incidenti), resposomica (capacità di risposta individuale) ed epigenomica (polimorfismi individuali) (Figura 45).
Lo Stress Ossidativo è stato più volte descritto come cofattore nella patogenesi delle infezioni virali (Figure 46-47). La somministrazione di FPP ha dimostrato, ad esempio, l’incremento della concentrazione delle IgA secretorie salivari e del lisozima (Figura 48)mentre nel liquido di lavaggio delle cavità nasali ha determinato l’up-grade dell’espressione di geni ad azione detossificante (Figura 49).
La nutrizione dimostra dunque di avere effetti molto importanti sulla up- e down-regulation dell’espressione genica (Figura 50). Lo testimonia la semplice osservazione delle differenze epigenetiche riscontrabili a diverse età nei gemelli omozigoti (Figura 51). Possono dunque la nutraceutica e la nutrizione avere effetti epigenetici (Figura 52)?
In un recente congresso a Parigi è stato riportato che una dieta ricca di frutta e verdura protratta per due mesi in soggetti diabetici ha determinato una significativa diminuzione di alcuni marcatori di lipoperossidazione senza determinare alcun incremento dei livelli basali di fattori vitaminici come beta-carotene e vitamina C (Figura 53). Per contro, un analogo studio sui fumatori non aveva in precedenza evidenziato alcun effetto sul danno ossidativo del DNA(Figura 54), nè sull’attivazione genica (Figura 55).
Dunque nutrizione e nutraceutica non sono tutto ma certamente sono importanti come è certo che lo stress ossidativo è intimamente implicato nel processo patogenetico (Figura 56).
Nel diabete, ad esempio, l’impiego di FPP permette di avere livelli di glicemia basale e post-prandiale mediamente inferiori rispetto ai non trattati (Figura 57) ed il suo effetto di modulazione è stato dimostrato in dettaglio studiando specifici marcatori (Figure 58-59).
Resta evidente che nutrizione, nutraceutica e farmaci hanno target diversi nel ciclo vitale di un individuo: mentre le prime due sono particolarmente efficaci nella fase compresa tra l’omeostasi e lo stress metabolico, i farmaci sono determinanti quando quest’ultimo evolve in sindrome metabolica e procede verso patologie maggiormente complesse (Figura 60).
Perchè nutrizione e nutraceutica non hanno però sempre dimostrato e in modo univoco la loro efficacia nel contrastare le alterazioni dell’omeostasi? Un’ipotesi è che esistano soggetti più o meno reattivi al trattamento con micronutrienti antiossidanti per effetto di varianti genetiche che determiano le proteine implicate nell’assorbimento dei micronutrienti stessi(Figura 61) così da distinguere i soggetti in low, medium e high responders e da rendere indispensabile una personalizzazione degli interventi nutraceutici (Figure 62-65).
Sistemi efficaci di monitoraggio dell’omeostasi, valutazione e monitoraggio del rischio di malattia geneticamente determinato e impiego di nutraceutici unitamente all’adozione di corretti stili di vita concorrono tra loro nell’assicurare lo stato di salute dell’organismo rallentandone l’alterazione e l’evoluzione verso la condizione patologica (Figure 66-68).