Patologie Croniche Degenerative
La grande varietà di ricadute fisiopatologiche, generate nell’organismo da uno squilibrio REDOX, può spiegare perché lo Stress Ossidativo può partecipare alla patogenesi e alle complicanze di molteplici stati morbosi.
È sempre difficile dimostrare se lo Stress Ossidativo è la causa iniziale, se partecipa soltanto ai meccanismi patogenetici o se compare nel quadro fisiopatologico finale del processo. Se, perciò, è riduttivo pensare allo Stress Ossidativo come l’origine di tutte le malattie nelle quali esso si manifesta, è però sensato considerarlo come una delle concause e uno degli anelli importanti della catena patogenetica.
Valutare i livelli di Stress Ossidativo e cercare di contrastarlo, anche quando questo non è la causa iniziante della malattia, può consentire di porre ostacoli alla catena e limitare la progressione del danno.
Il coinvolgimento dello Stress Ossidativo in molteplici patologie è, perciò, argomento di studio molto attuale. Gli stati morbosi per i quali vi sono evidenze di un ruolo patogenetico importante sono assai numerosi e variegati.
La comprensione del preciso ruolo dello Stress Ossidativo nella fisiopatologia di uno o più stati morbosi è un aspetto cruciale sia dal punta di vista scientifico che clinico. Può avere ricadute immediate sull’atteggiamento terapeutico se vi è evidenza di un ruolo causale e patogenetico: in questo caso le reazioni ossidative devono essere opportunamente contrastate. Se, invece, emerge un ruolo di marcatore e/o fattore di rischio, la presenza di segni bioumorali di Stress Ossidativo avrà importanza diagnostica e prognostica e l’eventuale intervento avrà carattere soprattutto preventivo.
La ricerca clinica indirizza, pertanto, gli sforzi al chiarimento dei molteplici e diversi aspetti che lo Stress Ossidativo assume nelle varie patologie: aspetti che possono anche assumere il carattere della variabilità negli stadi successivi di una stessa malattia.
Negli ultimi decenni la scienza medica ha raggiunto cospicue evidenze sull’origine, l’evoluzione e la cura di molte malattie. Attualmente, sono prevalenti le patologie croniche degenerative, che per definizione non possono essere guarite, ma possono essere prevenute. L’implicazione dei radicali liberi come causa e/o effetto di numerose patologie, specie di tipo cronico-degenerativo, giustifica gli interventi mirati allo Stress Ossidativo, che possono rappresentare una valida opzione terapeutica, utile a rallentarne il decorso clinico.
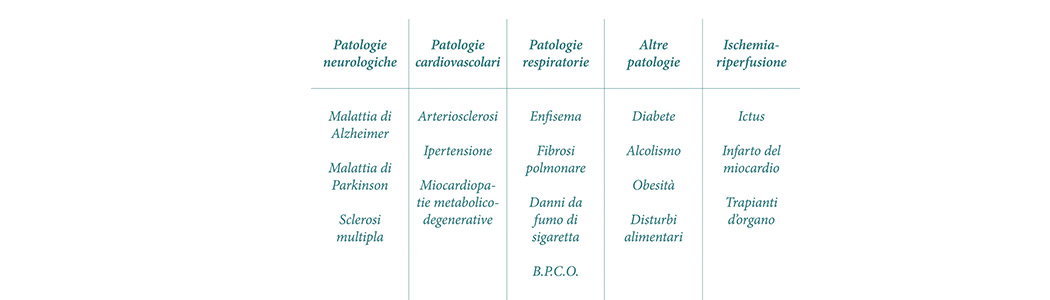
Nella tabella sono riportati numerosi stati morbosi, per i quali è stato invocato un meccanismo fisiopatologico di tipo flogistico che giustifica il richiamo allo stress ossidativo.
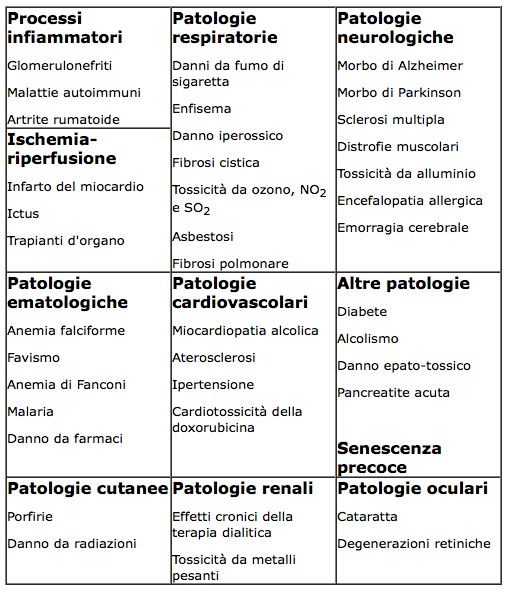
Nel corso di processi infiammatori, macrofagi e granulociti producono numerose sostanze, tra cui gli agenti ossidanti ROS e RNS: questi svolgono ruoli importanti e fisiologici di immunità “naturale” (azione tossica sui patogeni, coordinamento di reazioni immunitarie iniziali). D’altro lato, quando le specie ossidanti alterano l’equilibrio REDOX possono produrre effetti dannosi la cui intensità concorre ad originare fenomeni patologici. Tra essi Le patologie infiammatorie
Le Patologie Infiammatorie
- infiammazioni polmonari (sindrome stress respiratorio acuto – ARDS, malattia ostruttiva cronica – COPD, fibrosi polmonare) in cui ROS e RNS sono causa dinecrosi epiteliali e vascolari, degradazione del connettivo e attivazione dei fattori di trascrizione di interleuchine chemotattiche e proinfammatorie (IL-8) che alimentano e perpetuano il processo infiammatorio;
- artrite reumatodide: nel liquido sinoviale dei malati sono stati evidenziati aumentati livelli di F2-isoprostani derivati dalla perossidazione lipidica analoghi alle prostaglandine; inoltre, nei linfociti T isolati dalle articolazioni colpite sono stati evidenziati diminuiti livelli di GSH ridotto ed attivazione delle molecole di adesione.
Insufficienza renale cronica
Negli stati di insufficienza renale cronica sono state dimostrate alterazioni ossidative delle proteine e dei lipidi che causano l’accumulo plasmatico di aggregati macromolecolari (amiloidosi da dialisi) ed aterosclerosi precoce. Durante la dialisi, il solo contatto ematico con materiali scarsamente biocompatibili dei macchinari è causa di attivazione dei neutrofili, produzione di ROS e abbattimento del potenziale antiossidante aggravato dalla rimozione dell’acido urico dal circolo.
Diabete
Lo Stress Ossidativo sembra svolgere un ruolo significativo nella fisiopatologia del danno funzionale delle cellule beta pancreatiche: queste risultano particolarmente esposte al danno ossidativo anche perché nel diabete il potenziale antiossidante endocellulare risulta significativamente minore rispetto a quello di altri tipi cellulari.
Nel diabete tipo 1 le cellule beta sono bersaglio di un attacco autoimmune con invasione delle isole pancreatiche da parte di cellule mononucleate (insulite): la morte delle cellule insulari sembra mediata da macrofagi, cellule T e/o dall’esposizione a mediatori secreti dalle cellule stesse (citochine, ROS e NO).
Nel diabete tipo 2 l’iperglicemia, spesso associata ad iperlipidemia, causa un aumento di produzione mitocondriale di anione superossido e dei ROS che inducono l’ossido nitrico sintetasi inducibile (iNOS), oltre a produzione di NO ed anione perossinitrito citotossico che agiscono con effetti tossici sulle cellule beta.
Nel paziente diabetico i livelli di vitamine E e C sono generalmente diminuiti per effetto di uno squilibrio REDOX di origine probabilmente mitocondriale, dove l’iperglicemia genera ROS direttamente ed indirettamente mediante l’attivazione di alcune attività enzimatiche (NADPH ossidasi, xantina ossidasi, lipossigenasi, NO sintetasi).
Ischemia e riperfusione
Nella riperfusione postischemica si assiste ad aumento massivo dei ROS, che può produrre un danno tissutale, particolarmente importante in condizioni croniche quali la miocardiopatia e l’encefalopatia ischemica. Lo stesso fenomeno concorre a determinare un danno tissutale renale nei pazienti reduci da shock prolungato.
Un moderato innalzamento dei ROS è presente già durante la fase ischemica, probabilmente a livello soprattutto mitocondriale. Dopo riperfusione, un sensibile incremento dei ROS è stato osservato per attivazione della xantina ossidasi (conseguenza dell’accumulo tissutale dei cataboliti purinici dell’ATP consumato durante la fase anossica, con produzione intracellulare di anione superossido e acqua ossigenata) e per adesione dei neutrofili agli endoteli danneggiati, loro attivazione e produzione di sostanze proossidanti extracellulari.
Patologie cardiovascolari
Nella cellula miocardica, l’attacco ossidativo altera la compartimentazione subcellulare dello ione Ca++, i cui aumentati livelli citoplasmatici sembrano presenti in diverse patologie caridiovascolari quali l’iperplasia intimale (arteriosclerosi), la vasocostrizione (ipertensione), il danno miocardico da ischemia-riperfusione e l’ipertrofia che prelude allo scompenso cardiaco.
E’ stato dimostrato che la lipoperossidazione della membrana sarcoplasmatica delle cellule muscolari causa inibizione dell’ATPasi calcio-dipendente e il rilascio di Ca++ nel citoplasma; inoltre, ROS e perossidi lipidici disaccoppiano la fosforilazione ossidativa ed alterano il trasporto del Ca++ a livello mitocondriale.
E’ oramai ben noto che le LDL ossidate, accumulandosi nello spazio intimale della parete arteriosa, attivano i macrofagi ed altri tipi cellulari con effetto pro-ossidante. Nella placca aterosclerotica i processi di Stress Ossidativo possono favorire la progressione delle lesioni con molteplici meccanismi: azione chemiotattica su cellule infiammatorie, alterazione del bilancio proteasi/antiproteasi nella matrice connettivale, proliferazione di fibroblasti, cellule muscolari lisce e fibro-miociti.
Lo Stress Ossidativo, infine, induce apoptosi nelle cellule miocardiche: fenomeni di perossidazione lipidica a livello di membrana mitocondriale interna destabilizzano l’associazione citocromo C-cardiolipina e causano la fuoriuscita del citocromo dai mitocondri, che è una nota modalità di innesco del processo apoptotico.
Cancerogenesi
Accanto alla componente genetica, lo Stress Ossidativo è uno dei meccanismi molecolari maggiormente invocati nella genesi dei tumori. Molteplici sono le evidenze che suggeriscono un ruolo rilevante dei radicali liberi nella formazione e nell’evoluzione della patologia neoplastica: specifici interventi terapeutici miranti ad incrementare il potenziale antiossidante possono essere efficaci nella prevenzione e nella gestione del decorso clinico.
Malattie neurodegenerative
Il sistema nervoso centrale (SNC) è particolarmente vulnerabile ai processi ossidativi a causa della elevata quantità di ossigeno richiesta dal metabolismo dei neuroni, del suo elevato contenuto di acidi grassi insaturi facilmente aggredibili dalla perossidazione (fosfolipidi di membrana) e dei significativi depositi di metalli REDOX-attivi (ferro, rame).
Malattia di Alzheimer (AD)
Nella malattia di Alzheimer (AD) l’accumulo della sostanza beta-amiloide si accompagna a gradi significativi di danno ossidativo: le forme oligomeriche di beta amiloide (più di quelle fibrillari) stimolano la formazione di acqua ossigenata e la perossidazione lipidica, forse in virtù della capacità ferro/rame/zinco-legante. Nell’AD vi è, anche, evidenza di aumentati livelli di malondialdeide, 4-idrossi-nonenale, proteine ossidate, DNA-ossidato, diminuiti livelli di acidi grassi insaturi e formazione di perossinitrito e di proteine nitrosate nelle cellule microgliali che circondano le placche fibrose.
Malattia di Parkinson (PKD)
Nella malattia di Parkinson (PKD) fenomeni di REDOX-cycling analoghi all’AD colpiscono i neuroni dopaminergici della substantia nigra mesencefalica, regione ricca di ferro: numerose interazioni complesse ed ancora poco chiarite coinvolgono nei processi degenerativi anche glutatione, NO e dopamina (a sua volta in grado di catalizzare reazioni ossidative di ferro e rame)
Sindrome Laterale Amiotrofica (SLA)
Nelle forme familiari di sindrome laterale amiotrofica (SLA) sono state descritte mutazioni a carico dell’enzima superossido dismutasi rame-zinco (SOD-1), anche se queste non appaiono coinvolte nella patogenesi.
Riassumendo:
In definitiva, anche se è poco probabile che lo Stress Ossidativo rappresenti sempre l’evento primario di un processo patologico degenerativo, appare certo che nel corso della malattia si verificano processi ossidativi che partecipano in modo sostanziale alla progressione del danno.
Controllare i livelli di stato Redox e quindi monitorare lo Stress Ossidativo con specifiche e mirate indagini bioumorali, anche quando i radicali liberi non sono la genesi primaria della malattia, può consentire di intervenire sulla catena patogenetica e limitare la progressione del danno.
Iscriviti alla newsletter
© Casa di Cura Privata Villa Margherita S.r.l. 2021
Designed by Teslathemes, Supported by WPmatic